Thông Tin Thuốc – Tháng 11/2024
22/11/2024Bệnh viện Phụ Sản Nhi Bình Dương
Hiểu về dị ứng penicillin, phản ứng chéo và lựa chọn kháng sinh trước phẫu thuật
Giới thiệu:
Dị ứng penicillin được báo cáo bởi 8–15% dân số Hoa Kỳ, nhưng có tới 95% các trường hợp dị ứng này không tương ứng với dị ứng thực sự khi được thử nghiệm. Với kiến thức mới nổi này, thuật ngữ mới được đặt ra để chỉ dị ứng penicillin vẫn chưa được đánh giá là nhãn dị ứng penicillin (PAL). Việc có PAL ở bệnh nhân đang phẫu thuật không phải là lành tính. Một bài báo hấp dẫn được công bố vào tháng 11 năm 2019 liên hệ nguy cơ có PAL với việc phát triển nhiễm trùng tại vị trí phẫu thuật (SSI). Với hơn 8.000 bệnh nhân dị ứng penicillin được xem xét và hơn một nửa trong số những bệnh nhân này mắc các bệnh lý chỉnh hình, các tác giả phát hiện ra rằng tỷ lệ mắc SSI tăng 50% ở những bệnh nhân báo cáo dị ứng penicillin hoàn toàn là do sử dụng kháng sinh thay thế beta-lactam (chủ yếu là clindamycin hoặc vancomycin). Trong phẫu thuật chỉnh hình, PAL là yếu tố chính thúc đẩy việc lựa chọn kháng sinh thay thế trong phẫu thuật, trong đó clindamycin được sử dụng thường xuyên nhất (OR 34,6, 95% CI 29,9–30,1, P <.005). Việc sử dụng các loại kháng sinh hàng thứ hai này dẫn đến tăng các bệnh nhiễm trùng liên quan đến chăm sóc sức khỏe bao gồm tăng 23% tỷ lệ mắc Clostridium difficile , tăng 14% tỷ lệ mắc Staphylococcus aureus kháng methicillin (MRSA) và tăng 30% tỷ lệ mắc Enterococcus kháng vancomycin (VRE). Trong một nghiên cứu theo dõi đa địa điểm khác, bệnh nhân dị ứng beta-lactam được dùng kháng sinh không phải beta-lactam thay vì kháng sinh beta-lactam có nhiều tác dụng phụ được báo cáo hơn đáng kể dưới dạng nhập viện trở lại vì cùng một loại nhiễm trùng, tổn thương thận cấp tính, C. difficile hoặc các tác dụng phụ liên quan đến thuốc khác (OR 3,2, 95% CI 1,28–7,89). Ngoài việc gây ra tỷ lệ mắc bệnh và tử vong đáng kể, SSI chiếm 34% tổng chi phí chăm sóc sức khỏe liên quan đến các bệnh nhiễm trùng liên quan đến chăm sóc sức khỏe, với chi phí ước tính có thể quy cho mỗi trường hợp là 20.000 đô la. Các thủ thuật chỉnh hình có nguy cơ đặc biệt do vật liệu cấy ghép dẫn đến cả xu hướng phát triển nhiễm trùng tăng lên và quá trình loại bỏ nhiễm trùng khó khăn hơn khi nó xảy ra. Trong bài đánh giá này, sự phổ biến của PAL được thảo luận cũng như cơ sở lo ngại liên quan đến phản ứng chéo giữa penicillin với cefazolin, các thành phần sinh miễn dịch của cefazolin và penicillin, và các hướng dẫn hiện hành về lựa chọn kháng sinh trước phẫu thuật trong bối cảnh PAL. Khi hiểu được các nguyên tắc này, các hướng dẫn mới được đề xuất để đánh giá dị ứng và xác định các lựa chọn kháng sinh phù hợp trong bối cảnh trước phẫu thuật.
Hiểu về dị ứng penicillin và phản ứng chéo:
Dị ứng penicillin được báo cáo ở khoảng 8–15% công chúng nói chung. Hơn 95% các trường hợp dị ứng được báo cáo này không có phản ứng quá mẫn tức thời hoặc qua trung gian IgE khi thực hiện xét nghiệm da. Điều này có thể là do bệnh nhân chưa bao giờ bị dị ứng ngay từ đầu hoặc dị ứng đã giảm; trên thực tế, khoảng 80% bệnh nhân bị dị ứng penicillin qua trung gian IgE mất độ nhạy cảm sau 10 năm.
Theo truyền thống, người ta đã báo cáo rằng cephalosporin (trong đó cefazolin là thế hệ đầu tiên) có phản ứng chéo lên tới 10% với penicillin. Điều này gây ra vấn đề trong bối cảnh phẫu thuật vì có bằng chứng cấp độ 1 chứng minh cefazolin là tác nhân kháng sinh tối ưu để dự phòng trước phẫu thuật do tính chọn lọc của nó đối với hệ vi khuẩn trên da, cơ chế diệt khuẩn, khả năng thấm nhanh và khả dụng sinh học tại vị trí phẫu thuật. Tỷ lệ phản ứng chéo 10% thường được trích dẫn giữa penicillin và cephalosporin chỉ dựa trên một số ít nghiên cứu ban đầu hiện đã bị bác bỏ dựa trên dữ liệu cấp cao hơn gần đây. Trong số các báo cáo này có hai nghiên cứu từ những năm 1970; hiện nay người ta biết rằng các cephalosporin được giới thiệu trước năm 1980 có một lượng nhỏ penicillin làm chất gây ô nhiễm, và kết quả của các nghiên cứu này không có kết luận nào xét theo thực tế này. Ngoài ra, bản chất và mức độ nghiêm trọng của các phản ứng được báo cáo không được ghi chép đầy đủ. Một nghiên cứu ban đầu khác báo cáo tỷ lệ tương tự là 8% của bất kỳ loại phản ứng dị ứng nào từ việc dùng cephalosporin ở những bệnh nhân bị dị ứng penicillin được liệt kê dựa trên khảo sát bệnh nhân tự báo cáo. Trong vài năm qua, các nghiên cứu mới đã phát hiện ra rằng tỷ lệ phản ứng chéo thực sự thấp hơn nhiều. Một nghiên cứu vào năm 2015 đã dùng cephalosporin thế hệ đầu tiên (83% cefazolin) cho 153 bệnh nhân bị PAL chỉ dẫn đến một phản ứng quá mẫn nhẹ (nổi mề đay). Trên thực tế, tỷ lệ phản ứng có hại từ việc dùng clindamycin đã được chứng minh là cao hơn (1,5%). Một nghiên cứu khác đã xem xét 413 bệnh nhân bị PAL, tất cả đều được dùng cefazolin và chỉ một trong số những bệnh nhân này có thể có phản ứng. Mặc dù không có tài liệu nào về phản ứng thực tế, nhưng điều này đã được suy ra từ một ghi chú trong hồ sơ gây mê trong khi phẫu thuật cho thấy việc dùng diphenhydramine khi bắt đầu một ca bệnh, có thể đã được dùng để dự phòng một cách hợp lý. Cuối cùng, một nghiên cứu gần đây được công bố vào năm 2021 đã chứng minh rằng trong số 452 bệnh nhân bị PAL đã trải qua xét nghiệm dị ứng, 0 trong số 452 bệnh nhân có kết quả xét nghiệm da dương tính khi xét nghiệm cụ thể với cefazolin hoặc ceftriaxone.
Việc xem xét lại cấu trúc hóa học ba chiều và các thành phần sinh miễn dịch của cả cefazolin và penicillin có thể hữu ích trong việc hiểu lý do tại sao tỷ lệ phản ứng chéo thực sự có thể gần bằng không như những nghiên cứu gần đây này gợi ý. Cephalosporin và penicillin đều được coi là beta lactam vì chúng có chung một vòng beta lactam cốt lõi ( Hình 1 ). Chúng khác nhau ở chỗ penicillin có vòng thiazolidine năm cạnh được thay thế bằng vòng dihydrothiazine sáu cạnh trong cephalosporin. Sau khi phân hủy, penicillin vẫn giữ nguyên vòng thiazolidine trong khi cephalosporin phân hủy cả vòng beta-lactam và vòng dihydrothiazine của chúng. Các sản phẩm phân hủy này tạo thành các thành phần sinh miễn dịch của các phân tử này và sự khác biệt trong quá trình phân hủy có thể giải thích tỷ lệ phản ứng chéo thấp. Hơn nữa, cefazolin có hai chuỗi bên (R1 và R2) có cấu trúc không khớp với bất kỳ beta lactam nào khác bao gồm penicillin ( Hình 1 ). Dị ứng thực sự với cefazolin cực kỳ hiếm (<1%) và thường đặc hiệu với các chuỗi bên của nó, không phải với vòng lõi chung.
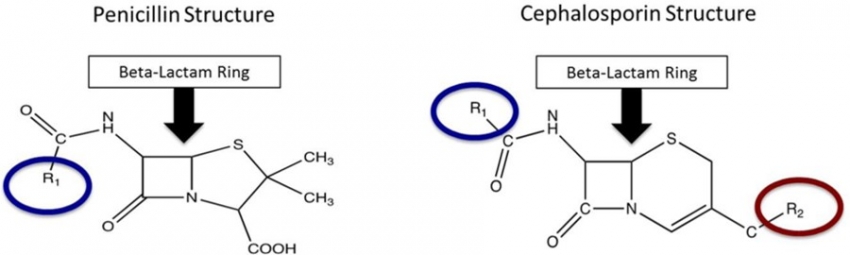
So sánh cấu trúc của cephalosporin và penicillin. Cephalosporin và penicillin đều chứa vòng beta-lactam lõi (mũi tên màu vàng). Cefazolin là cephalosporin thế hệ đầu tiên có chuỗi bên R1 và R2 tạo nên các thành phần miễn dịch chính, độc đáo và không giống với các beta lactam khác.
Công cụ phân tầng rủi ro mới được đề xuất:
Cephalosporin thế hệ đầu tiên, và đặc biệt là cefazolin, là tác nhân đầu tay được ưu tiên dựa trên mức bằng chứng cao nhất về kháng sinh trước phẫu thuật trong. Hướng dẫn của Viện Hàn lâm Phẫu thuật chỉnh hình Hoa Kỳ (AAOS) về dự phòng kháng sinh phản ánh điều này, nêu rằng nên sử dụng beta lactam thế hệ đầu tiên làm kháng sinh dự phòng trước. Về dị ứng beta-lactam, cần lưu ý rằng các lựa chọn thay thế cho bệnh nhân thực sự dị ứng penicillin bao gồm clindamycin và vancomycin mà không cần giải thích thêm. Hiện tại không có hướng dẫn hoặc công cụ phân tầng rủi ro nào khác để hướng dẫn bác sĩ phẫu thuật về lựa chọn kháng sinh trước phẫu thuật an toàn. Một nghiên cứu gần đây dựa trên dữ liệu về dị ứng và miễn dịch đã phát triển một phân tầng rủi ro được xác nhận cho những bệnh nhân trong bối cảnh đơn vị chăm sóc đặc biệt (ICU) bị PAL. Bệnh nhân được phân loại thành các nhóm rủi ro tùy thuộc vào phản ứng dị ứng đã báo cáo của họ. Trong số 184 bệnh nhân được coi là “nguy cơ thấp” dựa trên phản ứng được liệt kê của họ, không có bệnh nhân nào có kết quả xét nghiệm da dương tính với penicillin và không có triệu chứng nào sau khi dùng một liều cephalosporin thế hệ đầu tiên. Điều này dẫn đến giai đoạn thứ hai của nghiên cứu trong đó những bệnh nhân có nguy cơ thấp được dùng cephalosporin mà không cần xét nghiệm da; trong số 57 bệnh nhân liên tiếp đáp ứng tiêu chí này, tất cả đều dung nạp kháng sinh mà không có bất kỳ phản ứng nào.
Do đó, chúng tôi đề xuất một phiên bản được điều chỉnh của công cụ đã được xác thực này để các bác sĩ phẫu thuật ( Bảng 1 ) và ( Bảng 2 ) file đính kèm là “Bảng dị ứng chéo các kháng sinh ứng với sự tương đồng cấu trúc” cân nhắc khi quyết định lựa chọn kháng sinh trước phẫu thuật. Lựa chọn kháng sinh có thể được thực hiện dựa trên phân tầng rủi ro của phản ứng chỉ số được báo cáo của bệnh nhân với penicillin.
Bảng 1. Một công cụ phân tầng rủi ro được sửa đổi để lựa chọn kháng sinh trước phẫu thuật trong bối cảnh nhãn dị ứng penicillin
Giới thiệu:
Dị ứng penicillin được báo cáo bởi 8–15% dân số Hoa Kỳ, nhưng có tới 95% các trường hợp dị ứng này không tương ứng với dị ứng thực sự khi được thử nghiệm. Với kiến thức mới nổi này, thuật ngữ mới được đặt ra để chỉ dị ứng penicillin vẫn chưa được đánh giá là nhãn dị ứng penicillin (PAL). Việc có PAL ở bệnh nhân đang phẫu thuật không phải là lành tính. Một bài báo hấp dẫn được công bố vào tháng 11 năm 2019 liên hệ nguy cơ có PAL với việc phát triển nhiễm trùng tại vị trí phẫu thuật (SSI). Với hơn 8.000 bệnh nhân dị ứng penicillin được xem xét và hơn một nửa trong số những bệnh nhân này mắc các bệnh lý chỉnh hình, các tác giả phát hiện ra rằng tỷ lệ mắc SSI tăng 50% ở những bệnh nhân báo cáo dị ứng penicillin hoàn toàn là do sử dụng kháng sinh thay thế beta-lactam (chủ yếu là clindamycin hoặc vancomycin). Trong phẫu thuật chỉnh hình, PAL là yếu tố chính thúc đẩy việc lựa chọn kháng sinh thay thế trong phẫu thuật, trong đó clindamycin được sử dụng thường xuyên nhất (OR 34,6, 95% CI 29,9–30,1, P <.005). Việc sử dụng các loại kháng sinh hàng thứ hai này dẫn đến tăng các bệnh nhiễm trùng liên quan đến chăm sóc sức khỏe bao gồm tăng 23% tỷ lệ mắc Clostridium difficile , tăng 14% tỷ lệ mắc Staphylococcus aureus kháng methicillin (MRSA) và tăng 30% tỷ lệ mắc Enterococcus kháng vancomycin (VRE). Trong một nghiên cứu theo dõi đa địa điểm khác, bệnh nhân dị ứng beta-lactam được dùng kháng sinh không phải beta-lactam thay vì kháng sinh beta-lactam có nhiều tác dụng phụ được báo cáo hơn đáng kể dưới dạng nhập viện trở lại vì cùng một loại nhiễm trùng, tổn thương thận cấp tính, C. difficile hoặc các tác dụng phụ liên quan đến thuốc khác (OR 3,2, 95% CI 1,28–7,89). Ngoài việc gây ra tỷ lệ mắc bệnh và tử vong đáng kể, SSI chiếm 34% tổng chi phí chăm sóc sức khỏe liên quan đến các bệnh nhiễm trùng liên quan đến chăm sóc sức khỏe, với chi phí ước tính có thể quy cho mỗi trường hợp là 20.000 đô la. Các thủ thuật chỉnh hình có nguy cơ đặc biệt do vật liệu cấy ghép dẫn đến cả xu hướng phát triển nhiễm trùng tăng lên và quá trình loại bỏ nhiễm trùng khó khăn hơn khi nó xảy ra. Trong bài đánh giá này, sự phổ biến của PAL được thảo luận cũng như cơ sở lo ngại liên quan đến phản ứng chéo giữa penicillin với cefazolin, các thành phần sinh miễn dịch của cefazolin và penicillin, và các hướng dẫn hiện hành về lựa chọn kháng sinh trước phẫu thuật trong bối cảnh PAL. Khi hiểu được các nguyên tắc này, các hướng dẫn mới được đề xuất để đánh giá dị ứng và xác định các lựa chọn kháng sinh phù hợp trong bối cảnh trước phẫu thuật.
Hiểu về dị ứng penicillin và phản ứng chéo:
Dị ứng penicillin được báo cáo ở khoảng 8–15% công chúng nói chung. Hơn 95% các trường hợp dị ứng được báo cáo này không có phản ứng quá mẫn tức thời hoặc qua trung gian IgE khi thực hiện xét nghiệm da. Điều này có thể là do bệnh nhân chưa bao giờ bị dị ứng ngay từ đầu hoặc dị ứng đã giảm; trên thực tế, khoảng 80% bệnh nhân bị dị ứng penicillin qua trung gian IgE mất độ nhạy cảm sau 10 năm.
Theo truyền thống, người ta đã báo cáo rằng cephalosporin (trong đó cefazolin là thế hệ đầu tiên) có phản ứng chéo lên tới 10% với penicillin. Điều này gây ra vấn đề trong bối cảnh phẫu thuật vì có bằng chứng cấp độ 1 chứng minh cefazolin là tác nhân kháng sinh tối ưu để dự phòng trước phẫu thuật do tính chọn lọc của nó đối với hệ vi khuẩn trên da, cơ chế diệt khuẩn, khả năng thấm nhanh và khả dụng sinh học tại vị trí phẫu thuật. Tỷ lệ phản ứng chéo 10% thường được trích dẫn giữa penicillin và cephalosporin chỉ dựa trên một số ít nghiên cứu ban đầu hiện đã bị bác bỏ dựa trên dữ liệu cấp cao hơn gần đây. Trong số các báo cáo này có hai nghiên cứu từ những năm 1970; hiện nay người ta biết rằng các cephalosporin được giới thiệu trước năm 1980 có một lượng nhỏ penicillin làm chất gây ô nhiễm, và kết quả của các nghiên cứu này không có kết luận nào xét theo thực tế này. Ngoài ra, bản chất và mức độ nghiêm trọng của các phản ứng được báo cáo không được ghi chép đầy đủ. Một nghiên cứu ban đầu khác báo cáo tỷ lệ tương tự là 8% của bất kỳ loại phản ứng dị ứng nào từ việc dùng cephalosporin ở những bệnh nhân bị dị ứng penicillin được liệt kê dựa trên khảo sát bệnh nhân tự báo cáo. Trong vài năm qua, các nghiên cứu mới đã phát hiện ra rằng tỷ lệ phản ứng chéo thực sự thấp hơn nhiều. Một nghiên cứu vào năm 2015 đã dùng cephalosporin thế hệ đầu tiên (83% cefazolin) cho 153 bệnh nhân bị PAL chỉ dẫn đến một phản ứng quá mẫn nhẹ (nổi mề đay). Trên thực tế, tỷ lệ phản ứng có hại từ việc dùng clindamycin đã được chứng minh là cao hơn (1,5%). Một nghiên cứu khác đã xem xét 413 bệnh nhân bị PAL, tất cả đều được dùng cefazolin và chỉ một trong số những bệnh nhân này có thể có phản ứng. Mặc dù không có tài liệu nào về phản ứng thực tế, nhưng điều này đã được suy ra từ một ghi chú trong hồ sơ gây mê trong khi phẫu thuật cho thấy việc dùng diphenhydramine khi bắt đầu một ca bệnh, có thể đã được dùng để dự phòng một cách hợp lý. Cuối cùng, một nghiên cứu gần đây được công bố vào năm 2021 đã chứng minh rằng trong số 452 bệnh nhân bị PAL đã trải qua xét nghiệm dị ứng, 0 trong số 452 bệnh nhân có kết quả xét nghiệm da dương tính khi xét nghiệm cụ thể với cefazolin hoặc ceftriaxone.
Việc xem xét lại cấu trúc hóa học ba chiều và các thành phần sinh miễn dịch của cả cefazolin và penicillin có thể hữu ích trong việc hiểu lý do tại sao tỷ lệ phản ứng chéo thực sự có thể gần bằng không như những nghiên cứu gần đây này gợi ý. Cephalosporin và penicillin đều được coi là beta lactam vì chúng có chung một vòng beta lactam cốt lõi ( Hình 1 ). Chúng khác nhau ở chỗ penicillin có vòng thiazolidine năm cạnh được thay thế bằng vòng dihydrothiazine sáu cạnh trong cephalosporin. Sau khi phân hủy, penicillin vẫn giữ nguyên vòng thiazolidine trong khi cephalosporin phân hủy cả vòng beta-lactam và vòng dihydrothiazine của chúng. Các sản phẩm phân hủy này tạo thành các thành phần sinh miễn dịch của các phân tử này và sự khác biệt trong quá trình phân hủy có thể giải thích tỷ lệ phản ứng chéo thấp. Hơn nữa, cefazolin có hai chuỗi bên (R1 và R2) có cấu trúc không khớp với bất kỳ beta lactam nào khác bao gồm penicillin ( Hình 1 ). Dị ứng thực sự với cefazolin cực kỳ hiếm (<1%) và thường đặc hiệu với các chuỗi bên của nó, không phải với vòng lõi chung.

So sánh cấu trúc của cephalosporin và penicillin. Cephalosporin và penicillin đều chứa vòng beta-lactam lõi (mũi tên màu vàng). Cefazolin là cephalosporin thế hệ đầu tiên có chuỗi bên R1 và R2 tạo nên các thành phần miễn dịch chính, độc đáo và không giống với các beta lactam khác.
Công cụ phân tầng rủi ro mới được đề xuất:
Cephalosporin thế hệ đầu tiên, và đặc biệt là cefazolin, là tác nhân đầu tay được ưu tiên dựa trên mức bằng chứng cao nhất về kháng sinh trước phẫu thuật trong. Hướng dẫn của Viện Hàn lâm Phẫu thuật chỉnh hình Hoa Kỳ (AAOS) về dự phòng kháng sinh phản ánh điều này, nêu rằng nên sử dụng beta lactam thế hệ đầu tiên làm kháng sinh dự phòng trước. Về dị ứng beta-lactam, cần lưu ý rằng các lựa chọn thay thế cho bệnh nhân thực sự dị ứng penicillin bao gồm clindamycin và vancomycin mà không cần giải thích thêm. Hiện tại không có hướng dẫn hoặc công cụ phân tầng rủi ro nào khác để hướng dẫn bác sĩ phẫu thuật về lựa chọn kháng sinh trước phẫu thuật an toàn. Một nghiên cứu gần đây dựa trên dữ liệu về dị ứng và miễn dịch đã phát triển một phân tầng rủi ro được xác nhận cho những bệnh nhân trong bối cảnh đơn vị chăm sóc đặc biệt (ICU) bị PAL. Bệnh nhân được phân loại thành các nhóm rủi ro tùy thuộc vào phản ứng dị ứng đã báo cáo của họ. Trong số 184 bệnh nhân được coi là “nguy cơ thấp” dựa trên phản ứng được liệt kê của họ, không có bệnh nhân nào có kết quả xét nghiệm da dương tính với penicillin và không có triệu chứng nào sau khi dùng một liều cephalosporin thế hệ đầu tiên. Điều này dẫn đến giai đoạn thứ hai của nghiên cứu trong đó những bệnh nhân có nguy cơ thấp được dùng cephalosporin mà không cần xét nghiệm da; trong số 57 bệnh nhân liên tiếp đáp ứng tiêu chí này, tất cả đều dung nạp kháng sinh mà không có bất kỳ phản ứng nào.
Do đó, chúng tôi đề xuất một phiên bản được điều chỉnh của công cụ đã được xác thực này để các bác sĩ phẫu thuật ( Bảng 1 ) và ( Bảng 2 ) file đính kèm là “Bảng dị ứng chéo các kháng sinh ứng với sự tương đồng cấu trúc” cân nhắc khi quyết định lựa chọn kháng sinh trước phẫu thuật. Lựa chọn kháng sinh có thể được thực hiện dựa trên phân tầng rủi ro của phản ứng chỉ số được báo cáo của bệnh nhân với penicillin.
Bảng 1. Một công cụ phân tầng rủi ro được sửa đổi để lựa chọn kháng sinh trước phẫu thuật trong bối cảnh nhãn dị ứng penicillin
| Rủi ro thấp | Rủi ro trung bình | Rủi ro cao | |
|---|---|---|---|
| • Tác dụng phụ/không dung nạp (triệu chứng đường tiêu hóa, đau đầu, đau nhức cơ, rối loạn tâm thần) • Phản ứng quá mẫn hạn chế (phát ban trên da tự khỏi, nổi mề đay >5 năm trước, ngứa) • Không đặc hiệu (phản ứng không rõ, phản ứng từ thời thơ ấu) |
• Quá mẫn lan tỏa hoặc phản vệ (sưng mặt hoặc cổ họng, phù mạch, khó thở, nổi mề đay <5 năm trước) | • Hội chứng Stevens Johnson hoặc hoại tử biểu bì nhiễm độc (loét lan tỏa, phồng rộp, mụn mủ) • Phản ứng quá mẫn đa cơ quan (tiền sử tổn thương thận hoặc gan) |
|
| Kế hoạch: | Cho cefazolin | Cân nhắc chuyển đến xét nghiệm dị ứng trong bối cảnh được lựa chọn. Cho clindamycin hoặc vancomycin. | Cho clindamycin hoặc vancomycin |
- Nguy cơ thấp - Bệnh nhân thuộc nhóm nguy cơ thấp bao gồm những bệnh nhân có phản ứng chỉ số là tác dụng phụ hoặc không dung nạp (triệu chứng đường tiêu hóa, đau đầu, triệu chứng cơ xương hoặc rối loạn tâm thần), phản ứng quá mẫn hạn chế (phát ban da tự khỏi, nổi mề đay hơn 5 năm trước, ngứa) hoặc thiếu thông tin (dị ứng không rõ hoặc phản ứng thời thơ ấu xa xôi). Những bệnh nhân này nên dùng cefazolin mặc dù có dị ứng penicillin đã nêu. Phần lớn bệnh nhân, khoảng 60%, thuộc nhóm này dựa trên sàng lọc ban đầu.
- Nguy cơ trung bình - Bệnh nhân thuộc nhóm nguy cơ trung bình là những bệnh nhân có tiền sử phản ứng quá mẫn lan tỏa hoặc phản vệ (sưng mặt và họng, phù mạch, khó thở, nổi mề đay dưới 5 năm). Những bệnh nhân này trong bối cảnh tự chọn nên được cân nhắc xét nghiệm dị ứng. Nếu bệnh nhân chưa được xét nghiệm dị ứng để loại bỏ PAL, thì họ nên dùng clindamycin hoặc vancomycin.
- Nguy cơ nghiêm trọng - Bệnh nhân thuộc nhóm nguy cơ nghiêm trọng là những bệnh nhân có phản ứng chỉ số đáng lo ngại về hoại tử biểu bì nhiễm độc hoặc Hội chứng Stevens Johnson (phồng rộp niêm mạc hoặc da, loét hoặc mụn mủ), hoặc những bệnh nhân lo ngại về tình trạng liên quan đến nhiều cơ quan (tiền sử tổn thương thận hoặc thận). Điều này xảy ra ở <0,5% bệnh nhân. Những bệnh nhân này nên được dùng clindamycin hoặc vancomycin.
- Lưu ý, tài liệu đã chứng minh rằng từ 112 đến 124 bệnh nhân được báo cáo là dị ứng penicillin sẽ cần được đánh giá dị ứng để ngăn ngừa một lần SSI. Tài liệu chỉnh hình đã tái tạo các con số tương đương với con số này và chứng minh việc sử dụng cefazolin tăng lên sau khi xét nghiệm dị ứng. Trong một nghiên cứu được thực hiện trên những bệnh nhân phẫu thuật thay khớp, tất cả những người được báo cáo là dị ứng beta-lactam đều được chuyển đến phòng khám dị ứng thuốc trước phẫu thuật để tối ưu hóa việc dự phòng bằng thuốc kháng khuẩn. Trong số những bệnh nhân được gửi đi xét nghiệm da penicillin, 99% bệnh nhân không bị dị ứng penicillin và tất cả đều được dùng cefazolin tại thời điểm phẫu thuật mà không có bất kỳ phản ứng phụ nào. Một nghiên cứu khác phát hiện ra rằng 97% bệnh nhân đã hết PAL sau khi xét nghiệm dị ứng và một phương pháp thay thế beta-lactam dẫn đến tỷ lệ nhiễm trùng khớp giả cao hơn đáng kể ngay cả khi được kiểm soát bởi các yếu tố rủi ro khác. Với số lượng bệnh nhân cần đánh giá tương đối thấp và hiệu quả của chương trình giới thiệu dị ứng để loại bỏ PAL khỏi hồ sơ bệnh nhân, việc giới thiệu một bệnh nhân trong nhóm nguy cơ trung bình đi xét nghiệm dị ứng có vẻ là một nỗ lực đáng giá. Người ta cũng cho rằng việc đánh giá dị ứng penicillin bằng xét nghiệm da có thể tiết kiệm chi phí cho các thủ thuật chỉnh hình và hệ thống chăm sóc sức khỏe, với dự đoán sẽ giảm thêm chi phí để đánh giá bệnh nhân PAL có nguy cơ thấp không cần xét nghiệm da.
- Hướng dẫn thực hành lâm sàng nêu rõ liều dùng chính xác của cefazolin là 2 g cho bệnh nhân người lớn hoặc 3 gam khi cân nặng lớn hơn 120 kg sau mỗi 4 giờ. Liều dùng cho trẻ em là 30 mg/kg. Liều dùng clindamycin là 900 mg cho bệnh nhân người lớn sau mỗi 6 giờ. Liều dùng cho trẻ em là 10 mg/kg. Liều dùng vancomycin là 15 mg/kg và cần dùng trước khi rạch da từ 60 đến 120 phút để đạt được nồng độ ức chế tối thiểu. Thời điểm dùng vancomycin đặc biệt quan trọng; trong nghiên cứu của Blumenthal và cộng sự, 97,5% bệnh nhân dùng vancomycin làm kháng sinh trước phẫu thuật đã không dùng thuốc trong khung thời gian khuyến cáo; thời điểm bắt đầu dùng thuốc trung bình là 24 phút trước khi gây mê, trong khi chỉ có 1,7% bệnh nhân không dùng cefazolin trong khung thời gian khuyến cáo.
- Kháng sinh nhóm Beta Lactam là nhóm kháng sinh lớn và hiện tại đang dùng ở Bệnh viện phụ sản nhi Bình Dương gồm có Penicillin (Amoxcilin), Cephalosporins (Cefixim, cephalexin, Cefotaxime, cefdinir, ceftriaxone, cefuroxim) và Carbapenems (Imipenem).
- 1.Stone CA, Trubiano J, Coleman DT, Rukasin CRF, Phillips EJ. The challenge of de-labeling penicillin allergy. Allergy 2020; 75(2):273–288. Doi: 10.1111/all.13848. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 2.Coleman DT, Stone CA Jr, Wei WQ, Phillips EJ. Readiness for penicillin allergy testing: perception of allergy label (PEN-PAL) survey. J Allergy Clin Immunol Pract 2020; 8(9):3180–3182. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 3.Blumenthal KG, Ryan EE, Li Y, Lee H, Kuhlen JL, Shenoy ES. The impact of a reported penicillin allergy on surgical site infection risk. Clin Infect Dis 2018; 66(3):329–336. Doi: 10.1093/cid/cix794. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 4.Coleman DT, Stone CA, Wei WQ, Phillips EG. Penicillin allergy labels drive perioperative prophylactic antibiotic selection in orthopedic procedures. J Allergy Clin Immunol Pract 2020; 8(10):3634–3636. Doi: 10.1016/j.jaip.20202.07.007. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 5.Bull AL, Worth LJ, Richards MJ. Impact of vancomycin surgical antibiotic prophylaxis on the development of methicillin-sensitive staphylococcus aureus surgical site infections: report from Australian Surveillance Data (VICNISS). Ann Surg 2012; 256:1089–1092. Doi: 10.1097/SLA.0b013e31825fa398. [DOI] [PubMed] [Google Scholar]
- 6.Berríos-Torres SI, Yi SH, Bratzler DW, et al. Activity of commonly used anti-microbial prophylaxis regimens against pathogens causing coronary artery bypass graft and arthroplasty surgical site infections in the United States, 2006–2009. Infect Control Hosp Epidemiol 2014; 35:231–239. Doi: 10.1086/675289. [DOI] [PubMed] [Google Scholar]
- 7.Yee J, Dixon CM, McLean AP, Meakins JL. Clostridium difficile disease in a department of surgery. The significance of prophylactic antibiotics. Arch Surg 1991; 126:241–246. Doi: 10.1001/archsurg.1991.091410260131019. [DOI] [PubMed] [Google Scholar]
- 8.MacFadden DR, DaDelfa A, Leen J, et al. Impact of reported beta-lactam allergy on inpatient outcomes: a multicenter prospective cohort study, Clin Infect Dis 2016;63:904–910. Doi: 10.1093/cid/ciw462. [DOI] [PubMed] [Google Scholar]
- 9.Blanca M, Torres MJ, Garcia JJ, et al. Natural evolution of skin test sensitivity in patients allergic to beta-lactam antibiotics. J Allergy Clin Immunol 1999; 103:918–924. Doi: 10.1016/s0091-6749(99)70439-2. [DOI] [PubMed] [Google Scholar]
- 10.McDanel J, Perncevich E, Diekema D, et al. Comparative effectiveness of beta-lactams versus vancomycin for treatment of methicillin-susceptible Staphylococcus aureus bloodstream infections among 122 hospitals. Clin Infect Dis 2015;61:361–367. Doi: 10.1093/cid/civ308. [DOI] [PubMed] [Google Scholar]
- 11.Charneski L, Deshpande G, Smith SW. Impact of an antibiotic allergy label in the medical record on clinical outcomes in hospitalized patients. Pharmacotherapy 2011; 31:742–747. Doi: 10.1592/phco.31.8.742. [DOI] [PubMed] [Google Scholar]
- 12.Shenoy ES, Macy E, Rowe T, Blumenthal KG. Evaluation and management of penicillin allergy: a review. JAMA 2019;321(2):188–199. Doi: 10.1001/jama.2018.19283. [DOI] [PubMed] [Google Scholar]
- 13.Stone CA, Trubiano JA, Phillips EJ. Testing strategies and predictors for evaluating immediate and delayed reactions to cephalosporins. J Allergy Clin Immunol Pract 2021; 9(1):435–444. Doi: 10.1016/j.jaip.2020.07.056. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 14.Joint Task Force on Practice Parameters; American Academy of Allergy, Asthma and Immunology; American College of Allergy, Asthma and Immunology; Joint Council of Allergy, Asthma and Immunology. Drug allergy: an updated practice parameter. Ann Allergy Asthma Immunol 2010;105(4):259–273. Doi: 10.1016/j.anai.2010.08.002. [DOI] [PubMed] [Google Scholar]
- 15.ASHP Therapeutic Guidelines: Clinical practice guidelines for antimicrobial prophylaxis in surgery. Clinical Practice Guidelines for Antimicrobial Prophylaxis in Surgery - therapeutic-guidelines-antimicrobial-prophylaxis-surgery.ashx Accessed January 20, 2021.
- 16.Prokuski L Prophylactic antibiotics in orthopaedic surgery. J Am Acad Orthop Surg 2008;16:283–293. Doi: 10.5435/00124635-200805000-00007. [DOI] [PubMed] [Google Scholar]
- 17.Herbert ME. Medical myth. Ten percent of patients who are allergic to penicillin will have serious reactions if exposed to cephalosporins. Culture and Medicine 2000;172:341. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 18.Romano A, Mayorga C, Torres MJ, et al. Immediate allergic reactions to cephalosporins: cross-reactivity and selective responses. J Allergy Clin Immunol 2000; 106:177–183. Doi: 10.1067/mai.2000.111147. [DOI] [PubMed] [Google Scholar]
- 19.Romano A, Valluzzi RL, Caruso C, Maggioletti M, Quarantino D, Gaeta F. Cross-reactivity and tolerability of cephalosporins in patients with IgE-mediated hypersensitivity to penicillins. J Allergy Clin Immunol Pract 2018; 6(5);1662–1672. Doi: 10.1016/j.jaip.2018.01.020. [DOI] [PubMed] [Google Scholar]
- 20.Dash CH. Penicillin allergy and the cephalosporins. J Antimicrob Chemother 1975; 1 (3 suppl):107–118. [DOI] [PubMed] [Google Scholar]
- 21.Petz LD. Immunologic reactions of humans to cephalosporins. Postgrad Med J 1971; 47 suppl:64–69. [PubMed] [Google Scholar]
- 22.Beltran RJ, Kako H, Chovanec T, Ramsh A, Bissonnette B, Tobias JD. Penicillin allergy and surgical prophylaxis: cephalosporin cross-reactivity risk in a pediatric tertiary care center. J Pediatr Surg 2015; 50:856–859. Doi: 10.1016/j.jpedsurg.2014.10.048. [DOI] [PubMed] [Google Scholar]
- 23.Goodman EJ, Morgan MJ, Johnson PA, Nichols BA, Denk N, Gold BB. Cephalosporins can be given to penicillin-allergic patients who do not exhibit an anaphylactic response. J Clin Anesth 2001; 13:551–564. [DOI] [PubMed] [Google Scholar]
- 24.Trubiano JA, Stone CA, Grayson ML, et al. The 3 Cs of antibiotic allergy-classification, cross-reactivity, and collaboration. J Allergy Clin Immunol Pract 2017; 5(6):1532–1542. Doi: 10.1016/j.jaip.2017.06.017. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 25.Solensky R: Penicillin allergy: immediate reactions. UpToDate https://www.uptodate.com/contents/penicillin-allergy-immediate-reactions?source=related_link#subscribeMessage. Accessed January 20, 2021.
- 26.Pichichero ME. A review of evidence supporting the American Academy of Pediatrics recommendation for prescribing cephalosporin antibiotics for penicillin-allergic patients. Pediatrics 2005;115(4):1048–1049. Doi: 10.1542/peds.2004-1276. [DOI] [PubMed] [Google Scholar]
- 27.Khan DA, Banerji A, Berstein JA, et al. Cephalosporin allergy: current understanding and future challenges. J Allergy Clin Immunol Pract 2019;7(7):2105–2114. Doi: 10.1016/j.jaip.2019.06.001. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 28.AAOS. Appropriate use criteria for the management of patients with orthopaedic implants undergoing dental procedures https://www5.aaos.org/uploadedFiles/PreProduction/Quality/AUCs_and_Performance_Measures/appropriate_use/auc-patients-with-orthopaedic-implants-dental-procedures.pdf. Accessed January 20, 2021. [DOI] [PubMed]
- 29.AAOS. Perioperative appropriate antibiotics https://aaos.org/quality/quality-programs/quality-toolkits/perioperative-appropriate-antibiotics/. Accessed January 20, 2021.
- 30.Stone CA, Stollings JL, Lindsell CJ, et al. Risk-stratified management to remove low-risk penicillin allergy labels in the ICU. Am J Respir Crit Care Med 2020; 201(12):1572–157. Doi: 10.1164/rccm.202001-0089LE. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 31.Li J, Markus P, Osmon D, Estes L, Gosselin V, Hanssen A. Reduction of vancomycin use in orthopedic patients with a history of antibiotic allergy. Mayo Clin Proc 2000; 75(9):902–6. Doi: 10.4065/75.9.902. [DOI] [PubMed] [Google Scholar]
- 32.McDanel DL, Azar AE, Dowden AM, et al. Screening for beta-lactam allergy in joint arthroplasty patients to improve surgical prophylaxis practice. J Arthroplasty 2017;32:S101–S108. Doi: 10.1016/j.arth.2017.01.012. [DOI] [PubMed] [Google Scholar]
- 33.Wyles C, Hevesi M, Osmon D, et al. 2019 John Charnley Award: Increased risk of prosthetic joint infection following primary total knee and hip arthroplasty with the use of alternative antibiotics to cefazolin: the value of allergy testing for antibiotic prophylaxis. Bone Joint J 2019; 101-B(6_Supple_B):9–15. Doi: 10.1302/0301-620X.101B6.BJJ-2018-1407.R1 [DOI] [PubMed] [Google Scholar]
- 34.Blumenthal KG, Yu Li, Banerji A, Yun BJ, Long AA, Walensky RP . The cost of penicillin allergy evaluation. J Allergy Clin Immunol Pract 2018; 6(3):1019–1027. Doi: 10.1016/j.jaip.2017.08.006. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 35.Sousa-Pinto B, Blumenthal KG, Macy E, et al. Penicillin allergy testing is cost-saving: an economic evaluation study. Clin Infect Dis 2020. Feb 28;ciaa194. Doi 10.1093/cid/ciaa194. [DOI] [PMC free article] [PubMed]
- 36.Lee RU. Penicillin allergy delabeling can decrease antibiotic resistance, reduce costs, and optimize patient outcomes. Fed Pract 2020. 37(10):460–465. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 37.Pagani NR, Moverman MA, Puzzitiello RN, Menendez ME, Barnes CL, Kavolus JJ. Preoperative allergy testing for patients reporting penicillin and cephalosporin allergies is cost-effective in preventing infection after total knee and hip arthroplasty. J Arthroplasty 2021; 36(2):700–704. Doi: 10.1016/j.arth.2020.08.045. [DOI] [PubMed] [Google Scholar]
- 38.Trubiano JA, Vogrin S, Chua KYL, et al. Development and validation of a penicillin allergy clinical decision rule. JAMA Intern Med 2020;180(5):745–752. Doi: 10.1001/jamainternmed.2020.0403. [DOI] [PMC free article] [PubMed] [Google Scholar]
| BẢNG DỊ ỨNG CHÉO KHÁNG SINH | |||||||||||||||||||||||||||||||||||||||||||||
| 1 | Amikacin | 1 | Amikacin | ||||||||||||||||||||||||||||||||||||||||||
| 2 | Ampicillin | 2 | Ampicillin | Chú thích: Cách lựa chọn kháng sinh thay thế khi có tiền sử dị ứng | |||||||||||||||||||||||||||||||||||||||||
| 3 | Amoxicillin | X | 3 | Amoxicillin | X | Nguy cơ cao - Không sử dụng | * | Nguy cơ 1-10% - Cân nhắc lợi ích, nguy cơ trước khi sử dụng | |||||||||||||||||||||||||||||||||||||
| 4 | Azithromycin | 4 | Azithromycin | Không có nguy cơ - Có thể sử dụng | ** | Nguy cơ 1-3% - Theo dõi chặt chẽ nếu tiền sử dị ứng với beta-lactam | |||||||||||||||||||||||||||||||||||||||
| 5 | Cefamandol | * | * | 5 | Cefamandol | Biên soạn: Tổ dược lâm sàng - Khoa Dược | |||||||||||||||||||||||||||||||||||||||
| 6 | Cefadroxil * | X | X | X | 6 | Cefadroxil * | |||||||||||||||||||||||||||||||||||||||
| 7 | Cephalexin * | X | X | X | X | 7 | Cephalexin * | ||||||||||||||||||||||||||||||||||||||
| 8 | Cefazolin * | X | X | X | X | X | 8 | Cefazolin * | |||||||||||||||||||||||||||||||||||||
| 9 | Cefepim | * | * | X | X | X | X | 9 | Cefepim | ||||||||||||||||||||||||||||||||||||
| 10 | Cefixim | * | * | X | X | X | X | X | 10 | Cefixim | |||||||||||||||||||||||||||||||||||
| 11 | Cefotaxim | * | * | X | X | X | X | X | X | 11 | Cefotaxim | ||||||||||||||||||||||||||||||||||
| 12 | Cefoperazon | * | * | X | X | X | X | X | X | X | 12 | Cefoperazon | |||||||||||||||||||||||||||||||||
| 13 | Cefoxitin | * | * | X | X | X | X | X | X | X | X | 13 | Cefoxitin | ||||||||||||||||||||||||||||||||
| 14 | Cefpidom | * | * | X | X | X | X | X | X | X | X | X | 14 | Cefpidom | |||||||||||||||||||||||||||||||
| 15 | Ceftazidim | * | * | X | X | X | X | X | X | X | X | X | X | 15 | Ceftazidim | ||||||||||||||||||||||||||||||
| 16 | Ceftriaxon | * | * | X | X | X | X | X | X | X | X | X | X | X | 16 | Ceftriaxon | |||||||||||||||||||||||||||||
| 17 | Cefuroxim | * | * | X | X | X | X | X | X | X | X | X | X | X | X | 17 | Cefuroxim | ||||||||||||||||||||||||||||
| 18 | Chloramphenicol | 18 | Chloramphenicol | ||||||||||||||||||||||||||||||||||||||||||
| 19 | Ciprofloxacin | 19 | Ciprofloxacin | ||||||||||||||||||||||||||||||||||||||||||
| 20 | Clarythromycin | X | 20 | Clarythromycin | |||||||||||||||||||||||||||||||||||||||||
| 21 | Clindamycin | 21 | Clindamycin | ||||||||||||||||||||||||||||||||||||||||||
| 22 | oxacillin or cloxacilin | X | X | * | X | X | X | * | * | * | * | * | * | * | * | * | 22 | oxacillin or cloxacilin | |||||||||||||||||||||||||||
| 23 | Cotrimoxazol | 23 | Cotrimoxazol | ||||||||||||||||||||||||||||||||||||||||||
| 24 | Daptomycin | 24 | Daptomycin | ||||||||||||||||||||||||||||||||||||||||||
| 25 | Doxycylin | 25 | Doxycylin | ||||||||||||||||||||||||||||||||||||||||||
| 26 | Ertapenem | * | * | ** | ** | ** | ** | ** | ** | ** | ** | ** | ** | ** | ** | ** | * | 26 | Ertapenem | ||||||||||||||||||||||||||
| 27 | Erythromycin | X | X | 27 | Erythromycin | ||||||||||||||||||||||||||||||||||||||||
| 28 | Fosfomycin | 28 | Fosfomycin | ||||||||||||||||||||||||||||||||||||||||||
| 29 | Gentamicin | X | 29 | Gentamicin | |||||||||||||||||||||||||||||||||||||||||
| 30 | Imipenem/cilastatin | * | * | ** | ** | ** | ** | ** | ** | ** | ** | ** | ** | ** | ** | ** | * | X | 30 | Imipenem/cilastatin | |||||||||||||||||||||||||
| 31 | Levofloxacin | X | 31 | Levofloxacin | |||||||||||||||||||||||||||||||||||||||||
| 32 | Meropenem | * | * | ** | ** | ** | ** | ** | ** | ** | ** | ** | ** | ** | ** | ** | * | X | X | 32 | Meropenem | ||||||||||||||||||||||||
| 33 | Metronidazole | 33 | Metronidazole | ||||||||||||||||||||||||||||||||||||||||||
| 34 | Moxifloxacin | X | X | 34 | Moxifloxacin | ||||||||||||||||||||||||||||||||||||||||
| 35 | Ofloxacin | X | X | X | 35 | Ofloxacin | |||||||||||||||||||||||||||||||||||||||
| 36 | Penicillin | X | X | * | X | X | X | * | * | * | * | * | * | * | * | * | X | * | * | * | 36 | Penicillin | |||||||||||||||||||||||
| 37 | Piperacillin/Tazobactam | X | X | * | X | X | X | * | * | * | * | * | * | * | * | * | X | * | * | * | X | 37 | Piperacillin/Tazobactam | ||||||||||||||||||||||
| 38 | Streptomycin | X | X | 38 | Streptomycin | ||||||||||||||||||||||||||||||||||||||||
| 39 | Ticarcillin/clavulanic | X | X | * | X | X | X | * | * | * | * | * | * | * | * | * | X | * | * | * | X | X | 39 | Ticarcillin/clavulanic | |||||||||||||||||||||
| 40 | Tetracylin | X | 40 | Tetracylin | |||||||||||||||||||||||||||||||||||||||||
| 41 | Tinidazole | X | 41 | Tinidazole | |||||||||||||||||||||||||||||||||||||||||
| 42 | Tobramycin | X | X | X | 42 | Tobramycin | |||||||||||||||||||||||||||||||||||||||
| 43 | Vancomycin | 43 | Vancomycin | ||||||||||||||||||||||||||||||||||||||||||
| Cách tra: Tra theo hàng ngang sau đó đến hàng dọc tương ứng với mỗi kháng sinh; VD: Tra dị dứng chéo của Tobramycin: Bước 1: Hãy tra hàng ngang thứ 42, Bước 2: Tra hàng dọc thứ 42 |
|||||||||||||||||||||||||||||||||||||||||||||
Tags
thông tin thuốc thong tin thuoc Thông Tin Thuốc – Tháng 11/2024 thong tin thuoc ?? thang 11 2024
Bài viết khác
- Thông Tin Thuốc – Tháng 12/2024
- Thông Tin Thuốc – Tháng 10/2024
- Thông Tin Thuốc – Tháng 09/2024
- Thông Tin Thuốc – Tháng 08/2024
- Thông Tin Thuốc – Tháng 07/2024
- Thông Tin Thuốc – Tháng 05/2024
- THÔNG TIN THUỐC THÁNG 4/2024
- THÔNG TIN THUỐC THÁNG 3/2024
- Thông Tin Thuốc – Tháng 02/2024
- Thông Tin Thuốc – Tháng 01/2024
